浙江树人大学生物与环境工程学院,浙江 杭州, 310015
摘 要:以苯肼作为起始原料,与乙酰乙酸乙酯环合反应得到吡唑醇,再以DMF为溶剂与三氯氧磷反应得到吡唑醛,然后吡唑醛经高锰酸钾氧化得到吡唑酸,吡唑酸经酰氯化反应得到吡唑酰氯,最后与5-苯基-2-氨基-1,3,4-噻二唑反应得到新化合物N-(5-苯基-1,3,4-噻二唑-2-基)-3-甲基-1-苯基-5-氯-4-吡唑甲酰胺,其结构均经IR、1H NMR、MS表征。初步的生物活性测定结果表明,该化合物具有一定的杀虫、抑菌活性。
关键词:吡唑;酰胺;噻二唑
[中图分类号]O626.21 [文献标识码]A [文章编号]
1 引言
吡唑酰胺类化合物具有良好的生物活性,包括杀螨活性、杀虫活性、杀菌活性、抗病毒、抗肿瘤等[1-4]。1883年,Knorr合成了1-苯基-3-甲基-5-吡唑啉酮,并用它合成含吡唑环的退热药安替比林(Antipyrine) [5],这引起了有机化学家对吡唑环化合物的兴趣。1946年,Thampson发现了2-吡唑-5-酮具有抑制植物生长的作用,1950年美国Rubbe公司开发出具有杀菌活性的吡唑类化合物,之后相继有专利和文献报道吡唑类化合物具有良好的农药活性。吡唑类化合物表现出的高效、低毒、广谱和结构多样性的特点[6],吡唑类衍生物作为杂环化合物中一个重要类别在新药研发领域更是具有重要地位,许多新型、高效、对环境友好的吡唑类衍生物的农药品种也应运而生。国内外的一些药物公司相继成功开发了数十个含吡唑环的除草剂、杀虫剂和杀菌剂等新品种。如杀虫剂吡螨胺(Tebufenpyrad)、氯虫酰胺(Chlorantraniliprole) 、锐劲特(Regent)等;杀菌剂吡噻菌胺(Penthiopyrad)、氟唑菌苯胺(Penflufen)、氟唑环菌胺(Ssedaxane)、氟唑菌酰胺(Fluxapyroxad)等[7-11]。直至今日新型吡唑酰胺类化合物的研发一直是新农药创制研究的焦点之一。
1,3,4-噻二唑类化合物是优良的药物中间体,因其高效、低毒,具有抗菌、抗病毒、抗肿瘤、抗抑郁、抗焦虑活性、调节植物生长等广泛的生物活性和药理活性,可以用来制备抗菌药、消炎药、植物生长调节剂、驱虫药、农药杀菌剂等 [12-13],如现已开发的农药噻酰菌胺、活化酯等[14]。因此,1,3,4-噻二唑化合物的研究成为绿色新农药及药物研究的一个热点。
利用生物活性叠加原理,将吡唑环衍生物结构和1,3,4-噻二唑五元杂环分子片段叠加,有望获得具有优良生物活性的化合物。吡唑酰胺化合物由于含有吡唑、酰胺等高活性结构基团,通常具有低毒、高效等优良且广泛的生物活性,将吡唑4位的酰基进行酰胺化反应的方式引入了1,3,4-噻二唑环,以考察其生物活性。
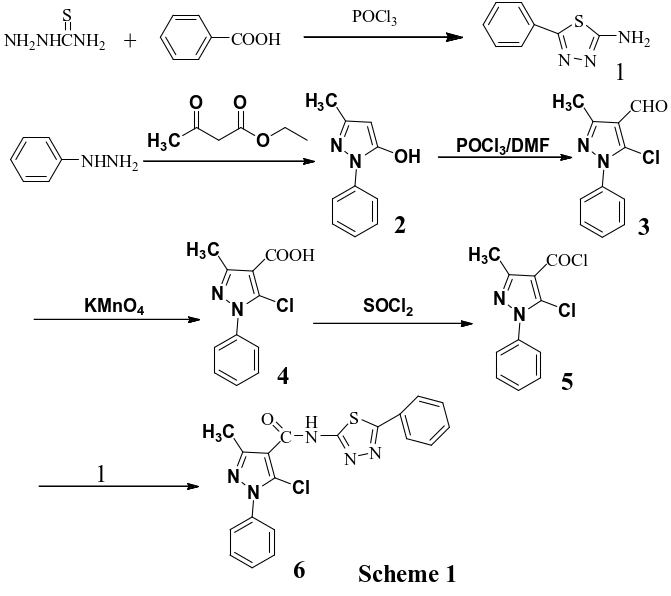
以苯肼为原料,经环合反应、醛基化反应、氧化反应得到中间体吡唑酸[15];然后酰氯化后与5-苯基-2-氨基-1,3,4-噻二唑缩合得到结构新颖的含噻二唑环的吡唑酰胺类化合物。对所合成的目标化合物进行生物活性测试。具体的合成路线如Scheme 1所示。
2 实验部分
2.1 实验仪器及药品
Bruker vector 22 红外光谱仪,HP-5989B型质谱仪,Bruker Avance 400 DMX核磁共振仪(TMS为内标, 溶剂用CDCl3),X-4型数字显示熔点测定仪(温度计未校正)。所用试剂均为分析纯。
2.2 化合物的合成
2.2.1 5-苯基-2-氨基-1,3,4-噻二唑(化合物1)的合成
在三口烧瓶(250 mL)中加入6.1 g苯甲酸,4.55 g氨基硫脲,16.5 mL POCl3,搅拌,装上冷凝管和温度计,加热至回流(温度大约为75℃),反应进行6 小时,冷却,至室温,在搅拌下,将反应液慢慢倾入40 g水+70 g冰的冰水中,冷却。用40%NaOH(质量分数)调pH值至8,趁热抽滤得黄色沉淀,用乙醇重结晶,干燥后得白色晶体。
2.2.2 3-甲基-1-苯基-5-吡唑啉酮(化合物2)的合成
在三口烧瓶(100 mL)中加入10.8 g苯肼,35 mL无水乙醇,搅拌溶解,加热至50 ℃,滴加14.3 g乙酰乙酸乙酯,滴毕回流,反应7 小时。稍冷,反应液倒入烧杯中,冷却至室温后,有固体析出,过滤,用大量水冲洗,滤饼干燥,得到黄色固体,收率90%以上。
2.2.3 3-甲基-1-苯基-5-氯-4-吡唑甲醛(化合物3)的合成 [11]
在三口烧瓶(250 mL)中加入15.5 mL DMF,搅拌,冰盐浴冷却到10 ℃以下,滴加23.3 mL POCl3,滴加温度控制在10 ℃以下,滴毕,去掉冰盐浴,向反应瓶中分批加入8.7 g化合物2,加毕,缓慢升温,100 ℃反应7小时。反应结束,将反应液稍冷,搅拌下,慢慢倾入碎冰中,有固体析出,过滤,用水洗涤,滤饼干燥,得到浅黄色固体,收率85%以上。
2.2.4 3-甲基-1-苯基-5-氯-4-吡唑甲酸(化合物4)的合成 [12]
在三口烧瓶(250 mL)中,加入11.03 g化合物3、10 mL丙酮和50 mL水,搅拌,缓慢升温至60 ℃,滴加高锰酸钾水溶液(高锰酸钾8.69 g,水100 mL),滴毕,加热80-85 ℃,保温反应4 小时,反应结束,冷却,滤液中慢慢加入浓盐酸至pH小于2,有大量白色固体析出,抽滤,蒸馏水洗涤至中性,滤饼干燥,得到白色固体,收率80 %以上。
2.2.5 3-甲基-1-苯基-5-氯-4-吡唑甲酰氯(化合物5)的合成
在单口烧瓶(100 mL)中,加入1.18 g化合物4和10 mL氯化亚砜,搅拌,加热至回流,反应2 小时,反应结束,浓缩除去过量的氯化亚砜,得到浅黄色液体,加入10 mL二氯甲烷,待用。
2.2.6 目标化合物(化合物6)的合成
在单口烧瓶(100 mL)中,加入0.90 g化合物1、8 mL三乙胺、10 mL二氯甲烷,搅拌,在0-5 oC下滴加待用的化合物5的二氯甲烷溶液,在室温下反应20 h。反应结束,用稀乙酸洗至中性, 分层, 有机相干燥、过滤、浓缩、柱层析分离得到纯品1.20 g,以化合物5计,反应收率为60.6%。
N-(5-苯基-1,3,4-噻二唑-2-基)-3-甲基-1-苯基-5-氯-4-吡唑甲酰胺,白色晶体;IR v(cm-1): 3310, 1670, 1538, 1420, 1275, 1140, 760; 1H NMR (CDCl3) δ: 2.25(s, 3H, CH3), 7.49-7.62(m, 8H, Ph-H) , 7.89-7.95(m, 2H, Ph-H), 8.42(s, 1H, NH); ESI-MS: 396.87[M+H]+, 398.93[M+H+2]+. Elemental anal. For C18H15ClN4O4(%), calculated: C, 57.65; H, 3.56; N, 17.69; found: C, 57.31; H, 3.77; N, 17.85.
2.3目标化合物生物活性测试
2.3.1 杀菌活性测试
(1)黄瓜霜霉病菌——普筛浓度200 mg/L
选择两张真叶期(摘去生长点)长势一致的盆栽黄瓜苗,喷雾处理后自然晾干,处理后24小时左右进行接种,取新鲜黄瓜霜霉病菌病叶,用毛笔蘸取10℃左右蒸馏水洗下病叶背面胞子囊,裴诚胞子囊悬浮液(2-3×105个/毫升)。用接种喷雾器(压力0.1MPa)在黄瓜苗上均匀喷雾接种,接种后的试材移至人工气候室,保持相对湿度100%,温度为15-20℃,24小时后保持温度15-24℃,相对湿度90%左右保湿诱发,五天后视空白对照发病情况进行分级调查,按病指计算防效。
(2)黄瓜白粉病菌——普筛浓度200 mg/L
选择一片真叶期、长势一致的黄瓜苗,喷雾处理后阴干24小时。洗取长满白粉菌黄瓜叶片上的新鲜孢子,用双层纱布过滤,制成孢子浓度为10万个/毫升左右的悬浮液,喷雾接种。接种后的试材自然风干,然后移至恒温室灯光下(21-23℃)中,7-8 天后视空白对照发病情况进行分级调查,按病指计算防效。
(3)黄瓜灰霉病菌——普筛浓度200 mg/L
采用叶片接菌法。选择二张真叶期长势一致盆栽黄瓜苗,待药剂喷雾晾干后,接菌饼于叶片上。22-26℃暗光保湿24毫升后,恢复自然光照培养约4天。待对照充分发病后用卡尺计量每个接种点病斑直径,计算防效。
(4)水稻纹枯病菌——普筛浓度200 mg/L
选择二张真叶期长势一致盆栽黄瓜苗,待药剂喷雾晾干后,将菌饼有菌丝的一面接贴于叶片上。22-26℃暗光保湿24小时后,恢复自然光照培养约4天。待对照充分发病后用卡尺计量每个接种点病斑直径,计算防效。
2.3.2 杀虫活性测试
(1)水稻褐飞虱筛选——培养皿苗虫定量喷雾法,普筛浓度500 mg/L
取培养皿,加少量水,将长3~4 cm的水稻苗用白石英沙固定于培养皿内,接用CO2麻醉的稻飞虱三龄中期若虫,置于POTTER喷雾塔下喷雾。喷雾后用透明塑料杯罩住,标记后放于观察室内。72 小时后检查结果。以空白CK对照。
(2)粘虫筛选——浸苗饲喂法,普筛浓度500 mg/L
将玉米叶在药液中充分浸润后自然阴干,放入培养皿中,接稻飞虱二龄中期幼虫,加盖标记后置于观察室内,72小时后检查结果。以空白CK对照。
(3)朱砂虫螨筛选——POTTER塔定量喷雾法,普筛浓度250 mg/L
将蚕豆叶片打成叶碟,背面朝上放在小块棉花上,置于塑料培养皿内,加少量水,接朱砂虫螨成螨。24小时后去除成螨,继续培养至五天后,将培养皿内水倒干,置于POTTER喷雾塔下喷雾,喷雾后加盖(中心有孔),标记后放于观察室内。24 小时后检查结果。以空白CK对照。
(4)苜蓿蚜筛选——POTTER塔定量喷雾法,普筛浓度250 mg/L
将蚕豆叶片剪去两端,背面朝上放在小块棉花上,置于塑料培养皿内,加少量水,接苜蓿蚜成蚜。24 小时后去除成蚜,继续培养至一天后,将培养皿内水倒干,置于POTTER喷雾塔下喷雾,喷雾后加盖(中心有孔),标记后放于观察室内。24小时后检查结果。以空白CK对照。
3 结果与讨论
3.1 目标化合物的谱学表征
该化合物的1H NMR谱图中的各个峰比较容易归属,吡唑环上甲基氢的化学位移在2.25 ppm,为单峰;苯环上的氢,化学位移在7.49 ppm和7.95 ppm之间出现;酰胺键上的氢,化学位移为8.42 ppm,显示为单峰。红外光谱中可以看到,在3310 cm-1处有NH吸收,在1670 cm-1处出现的强吸收峰为酰胺基上的C=O伸缩振动吸收峰。质谱给出的分子离子峰也与化合物的分子量相符。
3.2 目标化合物的生物活性研究
3.2.1 杀菌活性研究
采用盆栽活体测定法对合成的化合物进行了水稻纹枯菌(Rhizoctonia solani) 、黄瓜霜霉病菌(Pseudo-peronospora cubensis) 、黄瓜白粉病菌(Sphaerotheca fuliginea)和黄瓜灰霉病菌(Botrytis cinerea)的杀菌活性测定, 普筛浓度为200 mg/L。处理后定期观察记录叶片、植株的发病情况和菌丝生长情况,根据病情指数和菌丝直径,计算防效和抑制率。杀菌活性等级标准划分:A级—防效(抑制率)≥90%,B级—70%≤防效(抑制率)<90%,C级—50%≤防效(抑制率)<70%,D级—防效(抑制率)<50%。结果见表1。
结果表明,在试验浓度下,目标化合物具有一的抑菌活性,但其防效均在50%以下,对黄瓜白粉病菌的杀菌活性相对较好,其防效为49.61%。
表1 目标化合物的杀菌活性(抑制率/%)
Table1 The fungicidal activities of the compound (inhibition rate/%)
测试物质 | 黄瓜白粉病菌 | 黄瓜霜霉病菌 | 黄瓜灰霉病菌 | 水稻纹枯病菌 | ||||
防效 (%) | 毒力级别 | 防效(%) | 毒力级别 | 防效(%) | 毒力级别 | 防效 (%) | 毒力级别 | |
化合物6 | 49.61 | D | 16.76 | D | 11.90 | D | 23.83 | D |
blank | 0 | | 0 | | 0 | | 0 | |
3.2.2 杀虫活性研究
采用培养皿苗虫定量喷雾法对合成的化合物进行水稻褐飞虱(Nilaparvatalegen)的杀虫活性测定,普筛浓度500 mg/L;采用浸苗饲喂法对合成的化合物进行粘虫(Mythimaseparata)的杀虫活性测定,普筛浓度500mg/L;采用POTTER塔定量喷雾法对合成的化合物进行朱砂虫螨(Tetranychus cinnabarnus) 和苜蓿蚜(Aphismedicagini)的杀虫活性测定,普筛浓度250 mg/L。死亡率在90%以上为A级,70~90%之间为B级,50~70%之间为C级,0~50%之间为D级。结果见表2。
结果表明,在试验浓度下,目标化合物对苜蓿蚜、朱砂虫螨没有杀虫活性,对水稻褐飞虱、粘虫有一定的杀虫活性,但杀虫活性均低于50%。
表2 目标化合物的杀虫活性(死亡率/%)
Table2 The insecticidal activities of the compound (mortality rate/%)
测试物质 | 水稻褐飞虱 | 粘虫 | 朱砂虫螨 | 苜蓿蚜 | ||||
死亡率(%) | 毒力级 别 | 死 亡 率(%) | 毒力级 别 | 死亡率(%) | 毒力级 别 | 死亡率(%) | 毒力级 别 | |
化合物6 | 23.7 | D | 43.5 | D | 0 | D | 0 | D |
blank | 0 | | 0 | | 0 | | 0 | |
4 结论
以氨基硫脲、苯甲酸和三氯氧磷为原料,环合反应得到5-苯基-2-氨基-1,3,4-噻二唑中间体。以苯肼作为起始原料,与乙酰乙酸乙酯环合反应得到吡唑醇,再以DMF为溶剂与三氯氧磷反应得到吡唑醛,然后吡唑醛经高锰酸钾氧化得到吡唑酸,吡唑酸经酰氯化反应得到吡唑酰氯,最后与5-苯基-2-氨基-1,3,4-噻二唑反应得到新化合物N-(5-苯基-1,3,4-噻二唑-2-基)-3-甲基-1-苯基-5-氯-4-吡唑甲酰胺,粗品经柱层析等方法得到白色晶体,其结构均经IR、1H NMR、MS表征。初步的生物活性测定结果表明,目标化合物对黄瓜霜霉病菌、水稻纹枯菌、黄瓜霜霉病菌、黄瓜白粉病菌有一定的抑菌作用,杀菌活性均低于50%;在试验浓度下,目标化合物对水稻褐飞虱、粘虫具有一定的杀虫活性,但杀虫活性均低于50%。
参考文献
[1]程志明.新型杀螨剂—吡螨胺的开发[J].世界农药,2001,23(6): 18-23.
[2]赵恰,冯启,孔小林,等.1-苯基-1H-吡唑乙酰胺类化合物的合成及杀虫活性[J].农药,2015, 52(10): 728-730.
[3]翟志文,汪乔,沈钟华,等.新型含吡唑的三唑硫醚类化合物的合成与生物活性研究[J].有机化学,2016, 32: 1-5.
[4]欧阳贵平.新型吡唑类衍生物合成与抗病毒和抗癌生物活性研究[D]. 贵州,贵州大学,2008: 101-110.
[5]董浩,国媛媛,流程霖,等.吡唑类化合物的合成研究进展[J].化学通报,2017,80(2):46-50.
[6]张一宾,新颖杀虫杀螨剂—唑虫酰胺,世界农药,2003, 25(6): 43-45.
[7]杨国璋,新型吡唑类杀螨剂—腈吡螨酯,世界农药,2014, 36(6): 56.
[8]朱卫刚,胡伟群,张蕊蕊,陈杰,新型杀菌剂氟吡菌胺室内杀菌活性,农药,2012, 51(12): 922-924.
[9] 郑庆伟,加拿大拟批准登记氟啶胺和氟吡菌胺两种农药,农药市场信息,2015, 8(11): 50.
[10] 李梅,王振宁,宋宝安,胡德禹,吡唑类衍生物杀菌活性研究进展,农药,2008, 47(6): 391-395.
[11] 崔胜峰,王艳,吕敬松,噻唑类化合物应用研究新进展,中国科学:化学, 2012, 42(8): 1105-1131.
[12] 王辂,褚以文,噻唑肽类抗生素研究进展,中国抗生素杂志, 2008, 33(2): 69-74.
[13] 黄光, 杨吉春, 李慧超,等. 具有农药活性的噻唑类化合物的研究进展,农药, 2011, 50(2): 79-82.
[作者简介] 蒋含笑(1998-),男,杭州人,本科生;孙娜波(1975- ),女,慈溪人,指导老师,主要从事农药及中间体的合成,通讯作者。
[基金项目] 国家级大学生创新创业训练计划项目“吡唑酰胺类化合物的合成、杀菌活性筛选及手性拆分研究”(201911842015)
5